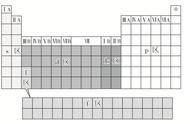
②根据元素金属性与非金属性可将元素周期表分为金属元素区和非金属元素区(如下图),处于金属与非金属交界线(又称梯形线)附近的非金属元素具有一定的金属性,又称为半金属或准金属,但不能叫两性非金属。

【特别提示】
“外围电子排布”即“价电子层”,对于主族元素,价电子层就是最外电子层,而对于过渡元素原子不仅仅是最外电子层,如Fe的价电子层排布为3d64s2。
2 . 对角线规则
在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的。

3 . 元素周期律
(1)原子半径
①影响因素
能层数:能层数越多,原子半径越大。
核电荷数:能层数相同,核电荷数越大,原子半径越小。
②变化规律
元素周期表中的同周期主族元素从左到右,原子半径逐渐减小;同主族元素从上到下,原子半径逐渐增大。
(2)电离能
①第一电离能:气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,符号:I1,单位:kJ/mol。
②规律
a.同周期:第一种元素的第一电离能最小,最后一种元素的第一电离能最大,总体呈现从左至右逐渐增大的变化趋势。
b.同族元素:从上至下第一电离能逐渐减小。
c.同种原子:逐级电离能越来越大(即I1<I2<I3…)。
(3)电负性
①含义:元素的原子在化合物中吸引键合电子能力的标度。元素的电负性越大,表示其原子在化合物中吸引键合电子的能力越强。
②标准:以最活泼的非金属氟的电负性为4.0作为相对标准,计算得出其他元素的电负性(稀有气体未计)。
③变化规律
金属元素的电负性一般小于1.8,非金属元素的电负性一般大于1.8,而位于非金属三角区边界的“类金属”(如锗、锑等)的电负性则在1.8左右。
在元素周期表中,同周期从左至右,元素的电负性逐渐增大,同主族从上至下,元素的电负性逐渐减小。
4 . 电离能、电负性的应用
(1)电离能的应用
①判断元素金属性的强弱
电离能越小,金属越容易失去电子,金属性越强;反之越弱。
②判断元素的化合价(I1、I2……表示各级电离能)
如果某元素的In+1≫In,则该元素的常见化合价为+n。如钠元素I2≫I1,所以钠元素的化合价为+1。
③判断核外电子的分层排布情况
多电子原子中,元素的各级电离能逐级增大,有一定的规律性。当电离能的变化出现突变时,电子层数就可能发生变化。
④反映元素原子的核外电子排布特点
同周期元素从左向右,元素的第一电离能并不是逐渐增大的,当元素的核外电子排布是全空、半充满和全充满状态时,第一电离能就会反常的大。
(2)电负性的应用

共价键
1.本质
在原子之间形成共用电子对(电子云的重叠)。
2.特征
具有饱和性和方向性。
3.分类