学了初中化学的朋友都知道,高炉炼铁的主要反应有
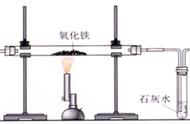
(1)氧化铁与一氧化碳在高温下反应生成铁和二氧化碳;
(2)碳和氧气反应生成二氧化碳,放出热量,为炼铁反应提供高温条件;
(3)碳与二氧化碳在高温下反应生成一氧化碳,吸热反应,为炼铁提供还原剂一氧化碳。
生产中炼制生铁所需焦炭的实际用量,远高于按照化学方程式计算所需的量,而且从高炉炉顶出来的气体中总是含有没有利用的 CO ,这是为什么呢?
开始,炼铁工程师们认为是 CO 与铁矿石接触不充分造成的,于是想方设法增加高炉的高度;然而,令人吃惊的是,高炉增高后,高炉尾气中 CO 的比例竟然没有改变。这便成了高炉炼铁技术中的一个科学悬念,人们一直在探究其中的原因……。
直到19世纪下半叶,炼铁高炉尾气之谜,法国化学家勒夏特列(1850--1936)经过深入的研究,才将这一谜底揭开。
原来,产生上述现象的原因是: 碳与二氧化碳的反应,在炼铁高炉中进行时,其实是一个可逆反应,并且自下而上发生在高炉中所有有焦炭的地方。后来的研究又证明,在高炉中铁的氧化物与一氧化碳的反应也不能全部转化为铁和二氧化碳;即为可逆反应。
上述这个事实充分说明,化学反应可逆是绝对的,不可逆是相对的。当一个反应的平衡常数大于10万时,即可认为该反应是不可逆的。另外,即使一个化学反应通常情况下是不可逆的,但在某些特定环境中发生就可能变成了可逆反应。
,