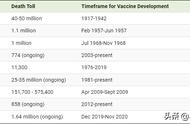
世卫组织工作人员和几内亚卫生官员开展的回顾研究确认,2013年西非埃博拉疫情的指示病例是住在几内亚Meliandou村的一名18个月大男孩
但激发出足够多的中和抗体,并不意味着一款疫苗就可以被批准上市了。抗体的出现只能说明人体免疫系统对疫苗起了反应,但这种反应是否足以保护接种者免受病毒的攻击?这种保护的有效率到底是多少?可以维持多长时间?以上这几个关键问题光凭Ⅱ期临床是无法知道的,因为真实环境中的病毒很可能通过一些我们不知道的办法躲过抗体的阻挠。
有些时候,抗体的存在甚至是有害的,反而会加重病情,这一现象被称为“抗体依赖增强效应”(Antibody-dependent Enhancement,简称ADE)。这个效应是在1966年进行的一次合胞病毒(Syncytial Virus)疫苗人体试验过程中首次被发现的,前期临床试验表明合胞病毒疫苗确实能诱导出抗体,但Ⅲ期临床试验却导致一大批受试者病情加重,两名儿童因此死亡。

5岁的小女孩凯特在出生六周后感染了呼吸道合胞病毒,这种病毒使得感染的婴幼儿需住院治疗
十多年后进行的一次登革热疫苗临床试验再次出现了这种情况,说明这个ADE效应不是偶然的,而是一种相当普遍的现象。科学家们经过仔细研究,发现登革热病毒有4种亚型,如果你对其中某一种亚型产生了抗体,但却又感染了另一种亚型的病毒,后者就会在前一种抗体的帮助下加速入侵人体的进程,导致更加严重的病情。
已知人类冠状病毒有7个亚型,除了几乎已经消失的SARS和目前尚未扩散开来的MERS之外,还有4种亚型能够导致普通的感冒,所以很多人体内应该已经有了针对某种冠状病毒的抗体。事实上,已有研究表明,在从未感染过新冠病毒的群体当中,有三分之一到一半的人体内能够检测到针对新冠病毒的免疫反应,原因很可能就是另外4种普通感冒病毒所导致的。但这样的免疫反应到底是会保护我们免受新冠病毒的困扰,还是会诱导出ADE,从而导致我们病得更加厉害呢?这个问题仅凭前期临床试验是无法解答的,必须进行更大规模的Ⅲ期临床试验才能找到答案。
话虽如此,前期临床试验测出的一些关于疫苗的基本免疫学指标还是很有用的,除了可以帮助科学家们确定Ⅲ期临床的接种剂量之外,还可以帮助疫苗研发者们对新冠疫苗的可行性做出合理的预判,从而决定是否值得继续做下去。
但即便证明能诱导出中和抗体,也已经是件大好事。要知道,并不是所有病毒都能诱导出抗体的,HIV病毒就是一例,所以艾滋病疫苗一直没能研发出来。普通感冒病毒往往也无法诱导出足够强的保护性抗体,这是因为大部分轻型感冒病毒都止步于上呼吸道,而人体免疫系统对于上呼吸道感染往往不怎么重视,不会诱导出强烈的免疫反应,否则的话我们就会天天生病了。

2013年,德国汉堡伯恩哈德·诺希特热带医学研究所的工作人员在研究埃博拉病毒
2020年新冠疫苗研发和试验早期,有媒体报道,新冠病毒诱导出的中和抗体滴度在病愈3个月后便急剧下降,甚至低到检测不出来了。这样的消息让很多读者感到绝望,但来自主流研究机构的顶尖免疫学家们纷纷站出来辟谣,指出病人痊愈后抗体水平急剧下降是正常现象,不值得大惊小怪。
原来,当病人痊愈后,大部分负责分泌抗体的B细胞都会死亡,所以抗体水平的下降是正常的。但是,会有一小部分B细胞转移进骨髓里,以“骨髓浆细胞”的形式潜伏下来。这些细胞虽然不再大量分泌抗体了,但它们仍然处于一种随时待命的状态,一旦再次遇到相同的外来抗原,它们就能迅速投入战斗,在短时间内生产出大量具有针对性的抗体,因此这些细胞又被称为“记忆细胞”,它们是“抗体免疫”的主力部队,也是疫苗之所以会有效的主要原因。
退一步讲,即使“抗体免疫”失效了,我们还可以依靠“细胞免疫”来保护自己,这项工作主要是由T细胞来完成的。T细胞种类繁多,功能也远比B细胞复杂得多。两种免疫细胞之间的互动更加复杂,甚至连一般的免疫学家也很难说得清楚。普通人只需记住两点就行了,那就是T细胞最主要的功能是找出并*死感染了病毒的人体细胞,而B细胞的主要功能是分泌抗体,防止病毒入侵。
如果用军事术语来做个比喻的话,我们可以将B细胞(及其分泌的抗体)看成是负责“扫街”的巡逻兵,需要直接和入侵敌军正面作战。而T细胞则相当于特种部队,最擅长挨家挨户搞搜查,把已经入侵成功并潜伏下来的敌人抓出来。我们当然希望在敌人潜入民居之前就将其抓获,所以由B细胞主导的“抗体免疫”的预防效果最好。但如果T细胞很厉害,能够把所有已被入侵的人体细胞都抓出来并消灭掉,我们也能满意。因此,起码从理论上讲,无论是“抗体免疫”还是“细胞免疫”都能起到保护作用。
甚至有研究表明,由T细胞主导的“细胞免疫”的记忆力要比由B细胞主导的“抗体免疫”更加持久。比如,今年距离“非典”已经过去了20年,大部分曾经感染过SARS的病人体内早已检测不到“非典”抗体了,但科学家在他们身上仍然发现了能够识别SARS表面抗原的T细胞,这些细胞仍然保留了那次“非典”感染留下的记忆。
虽然T细胞非常重要,但T细胞的研究难度要比抗体大得多,需要在专门的实验室里进行,耗时也更长,所以此前大部分疫苗研发工作都围绕着抗体来进行。但随着细胞研究技术的不断进步,越来越多的免疫学家开始关注T细胞免疫了。这次“新冠疫苗六杰”的前期临床试验全都检测了T细胞,结果发现受试疫苗都能激发出足够强的“细胞免疫”反应,这就进一步增强了疫苗研发者们的信心。这也是专业人士所说的疫苗即使不能避免感染,也能有效降低重症率的原因。
总之,新冠疫苗的前期临床表现,并没有出现太多反常规的地方。
Ⅲ期临床
所有的前期临床都是在严格控制的实验室条件下进行的,医生们清楚地知道自己在做什么,志愿者们也都知道自己接种的是哪类疫苗,可能会出现什么样的后果。但是,由于人体的代谢过程极为复杂,再加上安慰剂效应的存在,光凭实验室研究不足以证明疫苗安全有效,必须在真实的生活环境中进行大规模双盲对照试验才能得出肯定的结论,Ⅲ期临床试验就是为了这个目的而存在的。
以新冠疫苗为例,Ⅲ期临床至少需要招募数万名不同年龄、不同性别、不同身体状况的志愿者,先通过新冠抗体测试确保他们从来没有感染过新冠病毒,再将他们随机分成两组,一组按照Ⅱ期临床总结出来的最佳剂量接种受试疫苗,另一组则接种安慰剂。之后让这些志愿者回到自己的家中照常生活,但定期需要回到医院进行检查,看看这两组志愿者的新冠感染率是否有差别。
从这个流程来看,疫苗的Ⅲ期临床有两个难点需要克服:第一,试验地点必须具备良好的医疗基础设施,医护人员的水平也必须满足一定的要求,否则很难对这么多志愿者进行严格的监督和随访,最后得出的数据质量也不会令人满意。事实上,最近几年出现的新传染病大都是在非洲和西亚的一些发展中国家暴发的,当地医疗机构的水平达不到要求,只能从外面派医疗队去主持临床试验,难度非常大,这就是新疫苗迟迟无法通过Ⅲ期临床检验的最大原因。
第二,只有当对照组积累了一定的感染数之后,疫苗的Ⅲ期临床才能宣告结束,否则数据是没法用的。举例来说,假如某临床试验对照组1万人当中只有几个人感染,那么即使疫苗组无人感染,也说明不了什么问题,因为这个差别很可能是随机发生的,不能证明疫苗确实有效。但假如对照组1万人当中有数百人感染,疫苗组只有几个人感染,那就很能说明问题了。
要想在短时间内满足这一要求,疫苗所针对的传染病必须流行到一定程度才行。艾滋病疫苗之所以研发不出来,一个重要原因就是越来越普及的性卫生教育大大降低了HIV的感染率,导致艾滋病疫苗的Ⅲ期临床时间越拖越长,所需的接种人数越来越多,制药企业承受不起了。
当年“非典”疫苗的研发之所以被提前终止,也是因为隔离政策迅速控制住了疫情,科学家们根本找不到合适的人群进行Ⅲ期临床试验。此次新冠疫苗的Ⅲ期临床试验如果没有巴西和美国等疫情失控的国家存在的话,也是很难进行下去的,尤其是基础医疗设施相对健全的巴西更是成为各大疫苗研发公司的最爱。“新冠疫苗六杰”当中,科兴中维、牛津大学和德国BioNTech这3家均选择了巴西作为Ⅲ期临床的主要试验点,另外两家中国公司国药和康希诺则分别选择了同样疫情严重而基础设施相对完好的阿联酋和俄罗斯,莫德纳公司的Ⅲ期临床将在美国进行,牛津和BioNTech也把一部分Ⅲ期临床选在了美国。
在2020年进入Ⅲ期临床试验时,这几个国家看似疫情严重,但因为人口基数大,具体到每个人来说,被新冠病毒感染的可能性看起来也是不高的,研发者很可能需要等待很长的时间才能积累到一定的病例数。
举例来说,假设一种新冠疫苗的Ⅲ期临床招募了1.5万~2万志愿者,再假设这些人生活在一个年感染率为1%的地区(随着社交距离政策的广泛实施,如今这样的地区即使在美国和巴西也很难找到了),还要假设疫苗具有50%的有效率,那么半年之后研究人员将会发现大约150例确诊病例,勉强可以满足Ⅲ期临床的最低要求。
这种情况下,当时还有人提出可以招募一批志愿者充当“敢死队”,主动感染新冠病毒,以此来加快疫苗的研发进程。这个想法看似激进,其实在疫苗研发早期已经尝试过很多次了。当初詹纳第一次试验天花疫苗时就是拿自家园丁的8岁儿子做的试验,不过那是200多年前发生的事情,现在医疗界对伦理问题管得很严,不可能随便拿活人来做试验了。

(插图 老牛)
但新冠有几点比较特殊,一来这种病毒的致死率并不高,尤其是对于身体健康的中青年人来说,致死率远低于0.1%,如果只挑选这样的志愿者来参加试验,似乎还是可以接受的。二来新冠疫情对整个社会的影响太大了,哪怕早一天研发出疫苗,都能带来巨大的社会效益和经济效益,所以肯定有人愿意报名,研发者不愁招不到志愿者。牛津大学的疫苗研发团队就曾公开招募志愿者进行所谓的“人体挑战试验”(Human Challenge Trials),据说有3万人报了名。
虽然民间支持者众多,但还是有不少学者对这一做法表示了异议。美国哥伦比亚大学的病毒学家安吉拉·拉斯姆森(Angela Rasmussen)就认为,任何人体试验都必须把所有可能出现的情况如实告诉志愿者,这才是符合伦理道德的做法。但新冠是一种全新的传染病,后果难以预料,万一感染者出现了某种我们不知道的后遗症,或者疫苗诱发了前文提到过的“抗体依赖增强效应”,导致原本身体健康的年轻志愿者病情加重,研发团队是没办法交代的。另外,如果参加试验的都是身体健康的年轻人,那就无法知道这种疫苗对于身体虚弱的中老年人是否同样有效。再加上试验条件下的病毒感染剂量和感染方式很可能和真实情况有所不同,其结果就更说明不了问题了。
由于上述原因,“人体挑战试验”的作用很可能极其有限,最多只能作为一种辅助手段,弄不好反而会浪费宝贵的医疗资源。所以拉斯姆森认为我们不能把希望寄托在“人体挑战试验”上,还是得老老实实按部就班地进行真实情况下的Ⅲ期临床试验,这个时间是我们必须付出的代价。
疫苗批准太快还有一个坏处,那就是我们将无法知道疫苗的有效性到底能维持多久。如果一款疫苗只能为接种者提供3个月的保护期,每隔3个月都必须补打一针,那将严重影响全民免疫计划的实施。