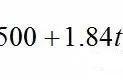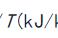符号约定:系统吸热“ ”,系统放热“—”
ds>0:吸热; ds<0:放热; ds=0:绝热
单位:J或KJ
热量也是过程量,示热图

功与热量的异同:
1、均为通过边界传递的能量;
2、均为过程量;
3、功传递由压力差推动,比体积变化是作功标志;
热量传递由温差推动,比熵变化是传热的标志;
4、功是系统与外界之间,在力的推动下,通过宏观有序运动而传递的能量;
热是系统与外界之间,在温度的推动下,通过微观无序运动而传递的能量;
功转化为热是无条件的;热转化为功是有条件、限度的。
七、热力过程和热力循环
热力循环分类:
1、按性质分:可逆循环;不可逆循
2、按目的分:正向循环;逆向循环
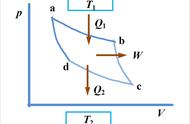
(一)正向循环(动力循环)特点:
1、输出净功;
2、在p-v图及T-s图上顺时针进行;
3、从高温热源吸热,向低温热源放热,同时向外输出功。

(二)逆向循环特点:(制冷循环、热泵循环)
1、输入净功;
2、在p-v图及T-s图上逆时针进行;
3、从低温热源吸热,向高温热源放热,并消耗功量。

(三)循环经济性评价指标: