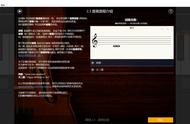
①该冰中的每个水分子有________个氢键;
②在气相中NH3易与H2O通过氢键以加合物形式存在,试写出加合物NH3·H2O的结构式:________________________________________________________________________
________________________________________________________________________。


2.锂—磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:

2Na3PO4+4CuSO4+2NH3·H2O===Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)写出基态Cu2+的核外电子排布式:__________________________________,
上述方程式中涉及到的N、O元素第一电离能由小到大的顺序为_______________________。
(2)PO的空间构型是_______________________________________。
(3)与NH3互为等电子体的分子、离子有___________________________________、
________________(各举一例)。
(4)氨基乙酸铜的分子结构如图1,碳原子的杂化方式为
________________________________________________________________________。
(5)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则1 mol [Cu(CN)4]2-中含有的σ键的数目为________。
(6)Cu元素与H元素可形成一种红色化合物,其晶体结构单元如图2所示,则该化合物的化学式为________________________________________________________________________。
答案 (1)[Ar]3d9 O<N
(2)正四面体
(3)PH3或AsH3 H3O+或CH
(4)sp3、sp2
(5)8NA
(6)CuH