原子结构

(1)所有元素的原子核都由质子和中子构成。
正例:612C 、613C 、614C三原子质子数相同都是6,中子数不同,分别为6、7、8。
反例:只有氕(11H)原子中没有中子,中子数为0。
(2)所有原子的中子数都大于质子数。
正例1:613C 、614C 、13H 等大多数原子的中子数大于质子数。
正例2:绝大多数元素的相对原子质量(近似等于质子数与中子数之和)都大于质子数的2倍。
反例1:氕(11H)没有中子,中子数小于质子数。
反例2:氘(11H)、氦(24He)、硼(510B)、碳(612C)、氮(714N)、氧(816O)、氖(1020Ne)、镁(1224Mg)、硅(1428Si)、硫(1632S)、钙
(3)具有相同质子数的微粒一定属于同一种元素。
正例:同一元素的不同微粒质子数相同:H 、H- 、H等。
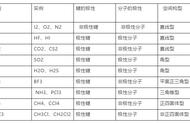
反例1:不同的中性分子可以质子数相同,如:Ne、HF、H2O、NH3、CH4 。
反例2:不同的阳离子可以质子数相同,如:Na 、H3O 、NH4 。
反例3:不同的阴离子可以质子数相同,如:NH4 、OH-和F-、Cl和HS。