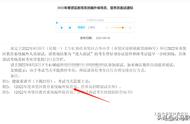
图六U3-1402治疗EGFR靶向药耐药患者的肿瘤变化瀑布图
可见所有患者肿瘤都有所缩小,T790M、C797S突变,CDK4、HER2扩增的患者的肿瘤都有缩小,而耐药机制不明确(灰色NE)的患者同样肿瘤有缩小。
U3-1402常见不良反应为恶心(60%),呕吐(40%),疲劳(33%),食欲减退(27%)和脱发(20%),大都是温和。严重不良反应为4级血小板计数降低,为剂量限制性毒性(6.4mg/kg)、3级发热性中性粒细胞减少。只有1例患者因为不良反应中止治疗,没有患者因为不良反应死亡。
ASCO大会研究点评专家建议未来可研究U3-1402联合EGFR靶向药或能提高疗效,而且专家还提出了大胆的想法,U3-1402可以从内部*死肿瘤细胞,有可能释放出肿瘤特异性抗原,将免疫系统无法识别的“冷”肿瘤变为免疫系统可以识别的“热”肿瘤,因此未来可以考虑研究U3-1402联合PD-1抑制剂。
TAK-788治疗EGFR 20外显子插入突变患者,客观缓解率43%TAK-788是日本武田医药开发的EGFR/HER2靶向药,可治疗治疗难治的EGFR 20外显子插入突变,在TAK-788的II期扩展研究中,共28例EGFR 20外显子插入突变患者,接受的治疗剂量为160mg,每天一次。
研究结果显示总体患者的中位无进展生存期为7.3个月,客观缓解率为43%,疾病控制率为86%。26例患者出现了不同程度的肿瘤缩小。有脑转移患者的客观缓解率为25%,疾病控制率为67%,而无脑转移患者的客观缓解率为56%,疾病控制率达到了100%。

图七 TAK-788治疗EGFR 20外显子插入突变疗效
安全性方面,常见不良反应包括腹泻、皮疹、恶心、呕吐、食欲下降及口腔炎,大多数不良反应可控。3级及以上严重不良反应包括腹泻、低钾血症、口腔炎及恶心,因不良反应导致停药的患者比例为10.7%。
目前TAK-788已经在中国大陆开展临床研究,值得关注。
AMG 510治疗KRAS突变,疾病控制率100%KRAS突变很早就被发现了,但几十年来一直找不到针对KRAS突变的有效药物。KRAS G12C突变是KRAS突变最常见的一个类型,13%的肺癌患者携带KRAS G12C突变。AMG 510是Amgen(安进)公司开发的针对KRAS G12C突变的口服小分子靶向药。美国FDA已经授予AMG 510治疗KARS G12C突变非小细胞肺癌和结直肠癌孤儿药资格。
目前AMG 510正在进行I期临床研究,研究分为4组不同剂量,分别为180mg、360mg、720mg和960mg,每天口服一次。现有10例参与研究的非小细胞肺癌患者可接受评估。 研究结果显示这10例患者中的5例肿瘤缩小至少30% , 这5例患者目前仍在接受AMG 510治疗。其余5例患者肿瘤都受到控制,疾病稳定。

图八 患者肿瘤变化瀑布图
可见接受不同剂量AMG 510治疗的患者均有疗效。
常见治疗期间出现的不良反应,包括食欲下降、腹泻、疲劳、头痛、咳嗽、潮热、恶心。6例患者治疗期间出现严重不良反应,但与AMG 510无关。没有观察到剂量限制性毒性,持续治疗也没有观察到毒性累积。
AMG 510的I期临床研究依然在招募患者,登记号NCT03600883。试验地点包括美国、加南大、韩国、澳大利亚。
DS-1062a“广谱”低毒,疾病控制率80%超过50%的非小细胞肺癌TROP2高表达,而且与生存期较短相关,这使TROP2成为一个理想的治疗靶点。DS-1062a是一种新型的靶向TROP2的抗体耦联药物,可以精准消灭TROP2表达的肿瘤细胞。
DS-1062a的 I期临床研究纳入了39例标准治疗无效的晚期非小细胞肺癌患者,分为8个组,分别接受由低到高剂量的DS-1062a治疗,目的是探索合适的剂量和初步的疗效。DS-1062a需要每3周静脉滴注一次。
研究结果显示4mg/kg及以上剂量DS-1062a对于化疗和靶向治疗难治的非小细胞肺癌有不错的疗效,至少40%的患者肿瘤缩小30%以上,80%的患者肿瘤控制良好。

图九 不同剂量DS-1062a治疗的肿瘤变化瀑布图
不同的颜色代表不同的剂量,可见大部患者的肿瘤都受到控制。
59.0%(23/39)的患者中出现了与药物相关的不良反应,其中91.3%(21/23)的患者 不良反应都是温和的1-2级。
最常见(≥3例患者)的治疗期间出现的不良反应包括恶心(n = 10);输液相关反应(n = 8); 疲劳(n = 7); 脱发(n = 6); 呕吐(n = 5); 贫血和皮疹(各4例);食欲下降和口腔炎(各3例)。
输液相关反应是温和的1级或2级能很好地控制。
25.6%(10/39)的患者治疗期间出现严重不良反应; 其中8例患者为3级,1例为5级,即死亡(败血症; 6 mg / kg给药组)。治疗期间的严重不良反应只有1例被认为与药物有关(发热,2级; 4.0 mg / kg给药组)。
6.mg / kg给药组患者出现一例剂量限制性毒性(斑丘疹,3级;已消退); 最大耐受剂量尚未探索到。
DS-1062a的I期临床试验依然在招募,登记编号NCT03401385。
Repotrectinib(TPX-0005),ROS1/NTRK双强,克服耐药控脑转
Repotrectinib(TPX-0005)是新一代ROS1 / NTRK / ALK靶向药,在I期临床研究TRIDENT-1中,Repotrectinib治疗先前未接受过任何靶向治疗的ROS1融合患者的客观缓解率高达82%,优于其他ROS1靶向药。