溶解度曲线是中考的必考点,也是同学们学习的难点。今天高分君给大家分享的就是关于溶解度曲线必须掌握的9个要点,帮助大家攻下这一考点。赶紧来看看吧!

一、溶解度曲线的应用

要点1:溶解度随温度的变化趋势
如:甲、乙的溶解度均随温度的升高而增大,丙的溶解度随温度的升高而减小 。
■ 方法指导:看曲线的坡度及走向,从左到右看曲线的走势是向上、向下还是平缓。向上表示随温度升高溶解度增大(如甲、乙);平缓表示随温度升高溶解度增大的趋势不显著(如乙);向下表示随温度升高溶解度减小(如丙)。
要点2: 溶解度曲线交点的含义
如:P点表示:t3℃时,甲、乙的溶解度相等,均为50 g 。
■ 方法指导:曲线交点表示该温度时,两种物质的溶解度相等,此时两种物质饱和溶液的溶质质量分数也相同。描述两条溶解度曲线交点所表示的意义时要指明温度。
要点3:溶解度大小的判断与比较
如:t1℃时,三种物质的溶解度由大到小的顺序为:丙>乙>甲 。
■ 方法指导:物质溶解度大小的比较离不开温度。过该温度对应的点作垂直于横轴的直线,看直线对应的交点的纵坐标:
①该纵坐标为此温度下对应物质的溶解度。
②针对两种或两种以上物质溶解度大小的比较,纵坐标越大,溶解度越大。
要点4:饱和溶液与不饱和溶液的判断及相互转化
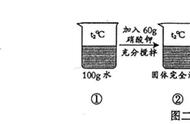
如:①t1℃时,将25 g甲物质加入到100 g水中,恰好形成甲的饱和溶液。②甲的饱和溶液升温后变成不饱和溶液。
■ 方法指导:
在一定温度下:
饱和溶液与不饱和溶液的转化:
①溶解度随温度的升高而增大,则
②溶解度随温度的升高而减小,则
要点5: 溶液溶质质量分数的计算与比较
如:t1℃时,将40 g丙加入到100 g水中,充分溶解,所得溶液的溶质质量分数为28.6%;t2℃时,甲的饱和溶液的溶质质量分数为20% 。
■ 方法指导:计算公式需谨记:
要点6:判断物质结晶的方法
要点7: 温度改变时,溶液中各种量的变化情况
如:t3℃时,将相同质量的甲、乙、丙的饱和溶液同时降温到t1℃,则下列说法正确的是(C )
A. 溶质质量分数:乙<丙
B. 溶剂质量:甲>乙
C. 溶质质量:乙>丙
D. 溶液质量:甲>丙
■ 方法指导:饱和溶液温度变化时:
(1)物质的溶解度随温度的升高而增大(即曲线为上升型)。
① 若将饱和溶液降低温度,由于析出晶体,溶液中溶质质量减小,溶剂质量不变,溶液质量减小,因此溶质质量分数变小。
② 若将饱和溶液升高温度,饱和溶液变为不饱和溶液,溶液中溶质、溶剂质量均不变,因此溶质质量分数也不变。
(2)物质的溶解度随温度升高而减小(即曲线为下降型)。改变温度时,溶液中溶质、溶剂、溶液的质量,溶质质量分数变化情况与上述分析相反。
二、溶解度表

要点1:从表中直接读取信息
(1)同一物质,不同温度下的溶解度。
如氯化钠在10℃时溶解度为35.8g,在30℃时溶解度为36.3g。
(2)不同物质,在同一温度下的溶解度。
如20℃时,氯化钠的溶解度为36.0 g,硝酸钾的溶解度为31.6g,氢氧化钙的溶解度为0.165 g。
(3)根据不同温度下溶解度的变化情况,判断物质的溶解度随温度的变化趋势。 如氯化钠的溶解度变化趋势为随温度升高,溶解度增大,但是幅度较小;硝酸钾的溶解度变化趋势为随温度升高增长幅度较大;氢氧化钙的溶解度变化趋势为随温度增大而减小 。(仅变化趋势、不做数据对比)
要点2:溶解度表的应用
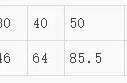
以表格数据形式考查两种物质(如NaCl和KNO3)溶解度相等的温度范围为20℃~ 30℃ 。
■ 方法指导:根据溶解度表,通过对比两种物质的溶解度,20℃以前,NaCl的溶解度大于KNO3,30℃以后,NaCl的溶解度小于KNO3,则NaCl和KNO3 溶解度相等的温度范围一定在20℃~ 30℃之间。
练一练
1. 如图是硝酸钾和氯化钠在不同温度时的溶解度曲线,下表是两种物质在部分温度时的溶解度数据。