知识点1 中和反应(重点)
1.探究酸、碱反应的实验
【实验目的】探究酸与碱能否发生反应
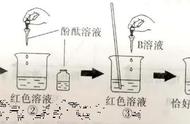
【实验过程】在烧杯中加入约5mL稀氢氧化钠溶液,滴入几滴酚酞溶液。用滴管向烧杯中慢慢滴入稀盐酸,并不断搅拌溶液,至溶液恰好变为无色为止(如图所示)。
【实验分析和结论】向氢氧化钠溶液中滴入几滴酚酞溶液,溶液变为红色,用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液恰好变成无色,说明氢氧化钠与盐酸恰好反应,但酸不要过量。发生反应的化学方程式:NaOH HCl NaCl H2O .
【易错点津】(1)做该实验时应注意,烧杯内要先盛放氢氧化钠溶液,然后滴加酚酞溶液,最好不要用石蕊试液,因为使用石蕊试液时溶液颜色变化不明显,不利于我们观察实验现象。
(2)采用此法判断无色的酸溶液和无色的碱溶液间是否发生了化学反应,反应是否完全,要注意操作时边滴加酸溶液边搅拌,否则不能说明“恰好”完全反应。
2.中和反应
(1)中和反应的概念:酸与碱作用生成盐和水的反应,叫做中和反应。例如:
Ca(OH)2 2HCl CaCl2 2H2O ; 2 NaOH H2SO4 Na2SO4 2H2O
(2)盐的概念:由金属离子(或铵根离子)和酸根离子构成的化合物,如NaCl、CaCl2、Na2SO4等。盐在水溶液中能解离出金属离子(或铵根离子)和酸根离子,如:NaCl Na Cl- ; Na2SO4 2Na SO42- .
【易错点津】我们平常所用的厨房调味品盐指的是食盐,也就是氯化钠(NaCl),而化学上所指 的盐是一类化合物的总称,就像酸、碱一样,这类化合物在水中都能解离出金属离子(或铵根离子)和酸根离子,像氯化钙(CaCl2)、碳酸钠(Na2CO3)、硫酸钾(K2SO4)等都属于盐类物质。
【规律方法】
水溶液中解离出的离子 特点 举例
酸 H 和酸根离子 阳离子全部是H HCl、H2SO4、HNO3
碱 OH-和金属离子 阴离子全部是OH- NaOH、Ca(OH)2 、
(或铵根离子) NH3·H2O
盐 金属离子(或铵根离子)
和酸根离子还可能含有其他离子 NaCl、K2SO4、NaHSO4
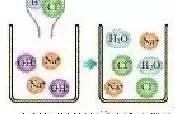
(3)中和反应的实质:中和反应的实质就是酸溶液中的H 与碱溶液中的OH- 结合生成水的过程。如反应:NaOH HCl=NaCl H2O,实际参加反应的是H 和OH- ,即H OH- H2O 。如图所示: