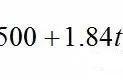变量变换法是在学科发展中形成的科学方法,通常在研究过程中会提出一些科学命题,为解决问题的思路或设计实验,总要想法进行命题的转换,以利用已有信息或通过实验进行分析,其间变量变换就是一个有效的方法。
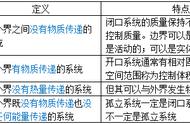
在物理化学中热力学量,不能确定其绝对值,也不能用实验直接测定,如热力学能(U)、焓(H)、熵(S)、亥姆霍兹自由能(A)、吉布斯自由能(G)等,而一些常用的量是可测的,如温度(T)、压力(p)等是可通过实验直接测量的热力学量。
热力学量变换法(简称变量变换法)就是将不能通过实验直接测得的量转换为用实验量或状态方程表示的关系的基本方法,变量变换的方法很多,如唐金(Donkin)定理法、雅可比(Jacobi)行列式法、塔玻尔斯基(Tobbl-sky)法、循环关系式法、Maxwell关系式法、系数比较法等。

它们的共同点是将目标问题进行等价转换,使抽象、复杂、不易实现的问题变得具体、简单、容易实现。
利用可测的热力学量来得到物理化学中的不可测的热力学量,物理化学中不可测的热力学量,如:

可由热力学基本方程和变量变换法得到,如利用可测的热力学量
(∂p/∂T)V、(∂V/∂T)p计算得到: