【预习反馈】
(1)玻意耳定律是英国科学家玻意耳和法国科学家马略特各自通过实验发现的。(✓)
(2)公式pV=C中的C是常量,指当p、V变化时C的值不变。(×)
(3)对于温度不同、质量不同、种类不同的气体,C值是相同。(×)
(4)在探究气体的等温变化实验中空气柱体积变化快慢对实验没有影响。(×)
(5)气体等温变化的p-V图象是一条倾斜的直线。(×)
【选一选】
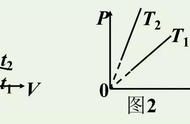
在下列各图中,表示压强,V表示体积,T为热力学温度,在图中能正确描述一定质量的气体不是等温变化的是(ABC)

【想一想】
借助铅笔,把气球塞进一只瓶子里,并拉大气球的吹气口,反扣在瓶口上,如图所示,然后给气球吹气,无论怎么吹,气球不过大了一点,想把气球吹大,非常困难,为什么?

解:由题意,“吹气口反扣在瓶口上”可知瓶内封闭着一定质量的空气,当气球稍大时,瓶内空气的体积缩小,根据气体压强、体积的关系,空气压强增大,阻碍了气球的膨胀,因而再要吹大气球是很困难的。
一、封闭气体压强的计算
【思考讨论】
例题:如图所示,玻璃管中都灌有水银,且水银柱都处在平衡状态,大气压相当于76cm高的水银柱产生的压强。

(1)静止或匀速运动系统中气体的压强,一般采用什么方法求解?
(2)图中被封闭气体A的压强各是多少?
解:(1)选择封闭气体接触的液柱(或活塞、气缸)为研究对象进行受力分析,列出平衡方程求解气体压强;
(2)①水银柱受内外气体的压力而平衡,故:p₁+ρgh=p₀,故p₁=71cmHg;
②闭气体压强小于大气压强,故气体压强为:
p₂=p₀-ρgh=76cmHg-10cmHg=66cmHg;
③闭气体压强大于大气压强,水银柱的竖直高度为h=10 cmxsin30°=5cm,气体压强为:p₃=p₀+ρgh=76cmHg+5cmHg=81cmHg;
④对于A部分气体压强为:pA=p₀-ρgh=76cmHg-5cmHg=71cmHg;
对于B部分气体压强,由图可得知,要比A部分的压强小,pB=pA-ρgh=71cmHg-5cmHg=66cmHg。
【旧纳总结】
1.容器静止时求封闭气体的压强
(1)求由液体封闭的气体压强,应选择最低液面(液面本身不计重力)列压强平衡方程。
(2)在考虑与气体接触的液柱所产生的附加压强时,应特别注意液柱产生的压强ρgh中的h是表示竖直高度(不是倾斜长度)。
(3)连通器原理:在连通器中同一液体(中间液体不间断的同一水平液面上压强是相等的。
(4)帕斯卡原理:液体会传递压强。
(5)求由固体封闭(如气缸或活塞封闭)气体的压强,应对此固体(气缸或活塞)进行受力分析,列合力平衡方程。
2.容器加速时求封闭气体的压强
恰当地选择研究对象,进行受力分析,然后依据牛顿第二定律列式求封闭气体的压强,把求解压强问题转化为动力学问题求解。
【典例剖析】
例题:如图所示,