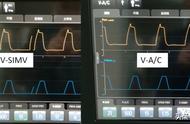
一旦确定某位患者需进行机械通气,需作出多种决定,包括选择机械通气模式。机械通气模式是指吸气性支持的方式。由于缺乏证据表明不同模式可影响临床结局,模式的选择一般取决于医生熟练度和机构偏好。
定容通气
定容通气(也称为容量控制通气或容量转换通气)需临床医生设定峰流速、流量模式、潮气量、呼吸频率、呼气末正压[positive end-expiratory pressure, PEEP;施加性(applied) PEEP,也称为外源性(extrinsic) PEEP],以及吸入氧分数(fraction of inspired oxygen, FiO2)。一旦达到设定的吸气时间,吸气结束。吸气时间和吸呼(I:E)比是由吸气峰流速决定的。增加吸气峰流速将减少吸气时间、增加呼气时间,并降低I:E比。气道压(峰压、平台压、平均气道压)取决于呼吸机的设置和患者相关的变量(例如:顺应性和气道阻力)。气道压高可能是由潮气量大、峰流量高、顺应性差[例如:急性呼吸窘迫综合征(acute respiratory distress syndrome, ARDS)、轻度的镇静]或气道阻力增加导致的(图 1和波形 1)。模式-定容通气可通过几种模式实现,包括控制性机械性通气(controlled mechanical ventilation, CMV)、辅助控制通气(assist control, AC)、间歇指令通气(intermittent mandatory ventilation, IMV)以及同步间歇指令通气(synchronized intermittent mandatory ventilation, SIMV)(表 1)。
CMV-在CMV模式中,每分钟通气量完全是由设定的呼吸频率和潮气量决定的。患者不会启动高于呼吸机设定的额外每分钟通气量。这可能是由于药物性麻痹、深度镇静、昏迷导致的,或由于所设定的每分钟通气量已达到或超过生理性需求,因此缺乏增加每分钟通气量的刺激。CMV无需患者进行做功。
AC-在AC模式中,临床医生通过设定呼吸频率和潮气量来确定最小的每分钟通气量。患者可通过触发额外的呼吸来增加每分钟通气量。每次由患者启动呼吸后,呼吸机均输出所设定的潮气量。举例如下。如果医生设定呼吸频率为20次/分钟,潮气量为500mL,那么最低可能的每分钟通气量是10L/min(20次呼吸/分钟×每次呼吸潮气量500mL)。如果在预设的20次呼吸之外,患者激发了5次额外的呼吸,那么呼吸机将为每次额外的呼吸提供500mL的潮气量,因此每分钟通气量将达到12.5L/min(25次呼吸/分钟×每次呼吸潮气量500mL)。
压力调节容量控制(pressure regulated volume control, PRVC)是一种容量控制通气,这种模式下设定潮气量,通过改变施加的气道压力以达到目标潮气量。根据前一次呼吸达到潮气量所需的压力改变而给予初始吸气压。在压力控制通气和PRVC中,吸气流都会随患者用力和肺力学而改变。可变气流对患者而言更舒适。对于特定的潮气量和肺顺应性,采用AC和PRVC模式平台压将相同。
间歇指令通气-IMV在两方面与AC类似:临床医生确定最低每分钟通气量(通过设定呼吸频率和潮气量),以及患者可增加每分钟通气量。然而,IMV模式在每分钟通气增加的方式上不同于AC模式。这具体是指,患者通过自主呼吸来增加每分钟的通气量,而不是通过患者启动的呼吸机呼吸。举例如下。如果临床医生设定呼吸频率为10次/分钟,潮气量为每次呼吸500mL,那么最低可能的每分钟通气量是5L/min(呼吸频率为10次/分钟×潮气量为每次500mL)。如果在预设的10次呼吸的基础上,患者启动额外的5次呼吸,那么每次额外呼吸的潮气量将取决于患者本身可产生的潮气量,其每分钟通气量将为大于5L/min的某一数值。精确的每分钟通气量取决于每次自发呼吸时潮气量的大小。SIMV-SIMV是IMV的另一种模式。在SIMV模式时,呼吸机的送气与患者的吸气用力是同步的。SIMV(或IMV)可在很大范围内调节通气支持的水平(图 2),这是这两种模式特有的优势。通气支持的范围可从完全支持(所设定的呼吸频率足够高,患者不会过度呼吸)至没有通气支持(所设定的呼吸频率为零)。如果正压通气导致发生血流动力学改变,可能需调整通气支持的水平。一项研究显示,当SIMV提供的支持水平低于50%时,心输出量、平均血压、肺毛细血管楔压和氧耗均更好。比较-SIMV和AC是最常使用的定容机械通气模式。与AC模式相比,SIMV可能的优势包括:人机同步性更好、呼吸肌功能的保留更好、平均气道压较低,以及可更大程度地控制通气支持的水平。此外,当进行SIMV时,可能较少产生内源性(auto)PEEP。相比之下,对于需使潮气量恒定或需完全或接近最大通气支持的危重患者,可能更适合采用AC模式。
定压通气
定压通气(也称为压力转换型通气)需临床医生设定吸气压的水平、I:E比、呼吸频率、PEEP(施加性PEEP)和FiO2。在达到设定的吸气压后停止送气。在定压通气时,潮气量是可变的。潮气量与吸气压的水平、顺应性、气道阻力和管道阻力有关。具体来说,当所设定的吸气压水平较高或顺应性良好,气道阻力小或呼吸机管道的阻力小时,潮气量将较大。相反,在定压通气期间,气道峰压是恒定的,其等于所设定的吸气压水平与外源性PEEP之和。例如,对于所设定的吸气压水平为20cmH2O,外源性PEEP为10cmH2O的患者,其气道峰压为30cmH2O。
定压通气可采用与定容通气相同的模式给予(表 1):在定压CMV(也称为压力控制通气)时,每分钟通气量完全取决于所设定的呼吸频率和吸气压水平。患者不会启动高于呼吸机设定的额外每分钟通气量。在定压AC时,所设定的呼吸频率和吸气压水平决定了最小每分钟通气量。患者可通过触发额外的、呼吸机辅助下的定压呼吸来增加每分钟通气量。在定压IMV或SIMV时,所设定的呼吸频率和吸气压水平决定了最小每分钟通气量。患者可通过启动自主呼吸来增加每分钟的通气量。
定容通气 vs 定压通气
在一项随机试验和几项观察性研究中,对定压通气和定容通气进行比较,结果发现:两种通气模式在死亡率、氧合或呼吸功方面的差异无统计学意义。与定容通气相比,定压通气的优势是:气道峰压较低、气体分布更均匀(区域性肺泡过度膨胀的情况更少)、人机同步性更好,以及可更早停用机械性通气。与定压通气相比,定容通气的优势是:只有定容通气可保持潮气量恒定,确保最低每分钟通气量。在大多数对定压通气和定容通气进行比较的研究中,对两种模式采用的均是方波(恒流)模式。当对含斜波(减速波)的定容机械性通气与定压通气进行比较时,气道峰压更低不再是定压通气的优势。
压力支持
压力支持通气(pressure support ventilation, PSV)是一种流量限制型通气模式,其可提供吸气压,直至吸气流量降至预设的其峰值的一个百分比时为止。该百分比通常是25%(图 3)。对于PSV,临床医生需设定压力支持的水平(吸气压水平)、外源性PEEP和FiO2。因为没有设定呼吸频率,患者必须自主触发每次呼吸。潮气量、呼吸频率和每分钟通气量取决于多种因素,包括呼吸机的设置和患者相关的变量(例如:顺应性、镇静的状态)。一般情况下,压力支持的水平较高可导致潮气量大且呼吸频率低。如果吸气流量足以满足患者的需求,呼吸功与压力支持的水平成反比。换句话说,增加压力支持的水平可减少呼吸功。呼吸功也与吸气流速成反比。增加吸气流速可缩短达到最大气道压的时间,这可降低呼吸功。潜在的用途-PSV似乎特别适合于机械性通气撤机,因为它往往是一种舒适的模式,患者可更好地控制吸气流速和呼吸频率。但临床研究未能显示PSV有助于撤机。PSV常与SIMV联用。呼吸机使用SIMV输出所设定的呼吸频率,而超出所设定的呼吸频率外的患者触发的呼吸是由PSV输出的。PSV启动的呼吸的目的,是克服气管内管和呼吸机回路的阻力。目前压力支持的必要水平尚未确定,通常是估算的。气管内管的阻力与管的直径和吸气流速有关。当采用直径小的气管内管(如,<7mm)时,压力支持的水平可能需大于等于10cmH2O以克服阻力。如果压力支持的水平高于克服阻力所需的水平,将增大潮气量。
缺点-PSV不太适合用于提供完全的或接近完全的通气支持。在此种情况下,PSV具有如下缺点:每次呼吸均必须由患者触发。如果由于镇静剂、病情危重或过度通气引起的低碳酸血症使呼吸驱动受到抑制,可能发生中枢性呼吸暂停。由于潮气量和呼吸频率可变,不能保证足够的每分钟通气量。当使用PSV进行完全通气支持时,可发生人机不同步,这可能使机械性通气的时间延长。与AC相比,PSV可导致睡眠更差。具体来说,当采用PSV时,患者在夜间第一阶段睡眠片段化的情况更多、1期和2期非快动眼睡眠相(non-rapid eye movement, NREM)睡眠更少、觉醒更多;在夜间第二阶段时,3期和4期NREM睡眠较少。在进行完全通气支持时,需相对高水平的压力支持(例如>20cmH2O),以防止肺泡萎陷(否则可导致周期性肺不张和呼吸机相关性肺损伤)和获得一种稳定的呼吸模式。如此高水平的压力支持不如中等水平压力(如10-15cmH2O)时舒适。虽然PSV一般不太适合用于提供完全或接近完全的通气支持,对于同时存在气道阻力增加[例如:慢性阻塞性肺疾病(chronic obstructive pulmonary disease, COPD)或哮喘发作]的患者,PSV尤其是一种很差的选择。当气道阻力较高时,每分钟通气量更可能不足,这可能与在输出比理想潮气量小的流量后,流量下降导致的吸气终止有关。此外,PSV几乎不能降低自发性(auto) PEEP[也称内源性(intrinsic) PEEP],内源性PEEP可增加患者的呼吸功并加重呼吸肌的疲劳。选择一种百分比较高的吸气流速峰值作为触发点终止吸气,可能稍微改善内源性PEEP。管道补偿-很多呼吸机可被设定为一种被称为自动管道补偿的模式。这种模式是一种类型的PSV,其可施加足够水平的正压来克服气管内管所引起的呼吸功,在每次呼吸中该呼吸功可有所不同。自动管道补偿常被用于自主呼吸试验。采用自动管道补偿进行自主呼吸试验的患者,比那些单纯接受持续气道正压(continuous positive airway pressure, CPAP)的患者更可能成功地耐受其试验。此外,许多呼吸机具有自动管道补偿与其他模式联用的选项,因此气管内管的阻力对通气没有影响。
持续气道正压
CPAP是指提供持续水平的气道正压,其在功能上类似于PEEP。在CPAP过程中,呼吸机无周期性通气变化,不提供高于CPAP水平的额外压力,所有呼吸均必须由患者触发。CPAP最常被用于治疗睡眠相关呼吸障碍、心源性肺水肿和肥胖低通气综合征。
双水平气道正压
双水平气道正压(bilevel positive airway pressure, BPAP)是一种在无创正压通气(noninvasive positive pressure ventilation, NPPV)期间使用的模式。BPAP可提供预先设定的吸气相气道正压(inspiratory positive airway pressure, IPAP)和呼气相气道正压(expiratory positive airway pressure, EPAP)。其潮气量与IPAP和EPAP之差有关。例如,当使用15cmH2O的IPAP和5cmH2O的EPAP(差值为10cmH2O)时,比使用10cmH2O的IPAP和5cmH2O的EPAP(差值为5cmH2O)时所产生的潮气量更大。大多数BPAP设备也允许设置备用呼吸频率。术语“BiPAP”常被误用来指代BPAP模式。BiPAP是美国Respironics公司生产的一种便携式呼吸机的名称,它仅是很多可提供BPAP的呼吸机中的一种。
气道压力释放通气
在气道压力释放通气(airway pressure release ventilation, APRV)过程中,先用较高的CPAP(高P)给予较长的持续时间(高T),之后降至较低的气道压(低P)且持续较短的时间(低T)(图 4和图 5)。高P向低P的转换可放出肺内的气体,并排出二氧化碳。相反,低P向高P的转换可使肺充气。高CPAP可使肺泡复张最大化。高P与低P间的压力差即为驱动压。差值越大,肺充气和放气越多;反之,差值越小,充气和放气越少。潮气量的确切大小与驱动压和顺应性均有关。高T和低T可决定充气和放气的频率。例如,对于将高T设定为5.4秒,低T设定为0.6秒的患者,其充气-放气周期持续6秒。这样每分钟可完成10次充气和放气。这种方法的大多数支持者认为应调整流速-时间波形以优化设置。理想情况下,调整呼气时间,从而在压力释放过程中呼气流速达到呼气峰流速(peak expiratory flow rate, PEFR)的75%左右时结束呼气。在高P和低P时均可能存在自主呼吸,但由于在低P时的时间较短,大部分自主呼吸发生在高P时。这是使APRV区别于其他反比通气(inverse ratio ventilation, IRV)模式的新特点。效果-目前尚未证实APRV可减少死亡率。然而,与其他通气模式相比,APRV改善其他重要的临床结局。在一项试验中,30例因创伤需进行机械性通气的患者被随机分配至2组:一组单纯接受APRV;一组在定压通气72小时后进行APRV。结果发现,单纯接受APRV的患者机械通气时间更短、入住重症监护病房(intensive care unit, ICU)的时间更短,且所需的镇静和麻痹药物更少。两组间的死亡率没有差异。另一项纳入148例ARDS患者的试验中,APRV使氧合和呼吸系统顺应性改善、平台压降低、不使用呼吸机天数更多和ICU住院时间缩短。在一项随机试验中,APRV产生了较大潮气量,通常超过12mL/kg理想体重,不过这种通气模式的最佳实施方案目前仍有争议。许多观察性研究表明,APRV可能降低气道峰压、改善肺泡复张、增加肺重力依赖区的通气并改善氧合。然而,此类发现并不是普遍存在的。在一项临床试验中,58例因急性肺损伤而接受机械通气的患者被随机分配至2组:一组接受APRV,一组接受SIMV加PSV。结果发现,两组患者在生理学或临床结局方面的差异没有统计学意义。在血流动力学方面,患者对APRV的耐受良好。一项试验纳入12例因ARDS而接受机械通气的患者,将患者从PC-IRV模式转为APRV模式。在PC-IRV模式期间,初始的高P为气道峰压的75%。当转变通气模式后,心脏指数和氧输送显著改善,并且对血管加压药的需求减少。虽然在这项试验中,大部分血流动力学的改善很可能与APRV期间的气道压比PC-IRV更低有关,但自主呼吸也具有血流动力学优势。
适应证-目前尚无被普遍接受的适应证。APRV及其相关模式[间歇指令气道压力释放通气(intermittent mandatory airway pressure release ventilation, IMPRV)和双水平间歇正压通气的应用,在ARDS患者中介绍得最清楚。理论上,APRV可使肺泡复张并改善氧合。
禁忌证-APRV及其相关模式很少用于存在重度阻塞性气道疾病或通气需求高的患者,因为可能导致肺过度充气、高肺泡压和肺气压伤。
相关模式-IMPRV和双水平间歇正压通气(在此被称为双水平通气)与APRV相似。具体来说,它们均允许进行自主呼吸,并且具有因高P与低P间转换引起的周期性充气和放气。在IMPRV时,周期性充气和放气被设定为在每隔几次自主呼吸后随呼吸同步发生。双水平通气和APRV的主要区别是,在双水平通气中低T的时间更长,从而允许在低P时可发生更多的自主呼吸(图 6)。另一个区别是,与双水平通气相比,更常使用APRV进行IRV。双水平通气也被称为Bi-Vent通气、BiLevel通气、BiPhasic通气和DuoPAP通气,其不同于BPAP(NPPV的一种常见类型)。
高频通气
高频机械性通气所采用的呼吸频率非常高,潮气量较低。此内容详见其他专题。
适应性支持通气
适应性支持通气(adaptive support ventilation, ASV)是一种通过调整呼吸力学,使之达到可满足希望的每分钟通气量所必要的呼吸频率和吸气压力的通气模式:对于不能触发呼吸机的患者,由机器给予压力控制呼吸。对于能够触发呼吸机的患者,对其触发的呼吸给予压力支持,并根据需要辅以压力控制呼吸,以达到所需的呼吸频率。作出这些调节的根据是公式,在给定每分钟通气量的情况下,该公式可确定使呼吸功最小化的呼吸频率。该公式依赖于呼气时间常数,该常数可从针对每次呼吸的流量容积环的呼气支获得。当采用ASV通气时,呼气时间常数较长的患者(如COPD)与呼气较快的肺部僵硬(如ARDS)或胸壁僵硬(如脊柱侧后凸、病态肥胖、神经肌肉疾病)患者相比,要采用更大潮气量和更低呼吸频率。尚未证实ASV对重要临床结局的作用比其他机械通气模式更好,但一项随机试验显示,采用ASV一定程度提前了撤机时间及缩短了撤机过程。
神经调节辅助通气
神经调节辅助通气(neurally adjusted ventilatory assist ventilation, NAVA)是一种尚处于研究阶段的通气模式,其采用膈肌放电[即膈肌兴奋;膈肌电活动(electrical activity of the diaphragm, EAdi)]来触发机械呼吸。当嵌入胃管的监测导管检测出EAdi信号的偏离超出设定阈值(通常为0.5μv)时,给予机械呼吸。辅助通气的程度随检出EAdi的振幅和临床医生设定的辅助通气水平而变化,因此每次呼吸的潮气量存在差异。辅助通气水平要在很短时间内凭经验调整后确定,将辅助通气水平增加至检测显示潮气量对患者而言舒适、恒定,而且EAdi信号保持平稳。NAVA的神经冲动-呼吸机耦合(即自主呼吸与输送机械呼吸之间的时间间隔)比传统机械通气模式快。因此NAVA有可能改善人机同步性,比如在COPD患者中。不过,虽然有小型非对照试验显示NAVA改善了人机不同步问题,但这些试验均未证实可改善有临床意义的结局,比如死亡或无呼吸机生存情况。NAVA的成功依赖于完整的呼吸驱动,即患者必须能够自主呼吸,对于呼吸驱动减弱甚至没有(比如深度镇静或颈脊髓损伤导致通气不足)的患者,这种通气模式并不适用。
反比通气
IRV不是一种机械性通气模式,而是一种在定容或定压机械性通气期间采用的策略。在IRV期间,吸气时间大于呼气时间(I:E比反向),这可增加平均气道压力并可能改善氧合。如果尽管给予最佳的PEEP和FiO2患者仍存在严重低氧血症,则可能需尝试IRV。研究从未证实IRV可改善重要的临床结局,如死亡、机械通气持续时间或ICU住院时间。多数证据表明IRV可改善氧合,但这些证据较弱且具有质量较低和研究结果不一致的特点。下述研究说明了目前已有的资料:一项纳入31例接受压力控制通气的患者的观察性研究发现,这些患者在开始IRV后,虽然PEEP降低,但其平均气道压力和PaO2(从69mmHg增加至80mmHg)显著增加。一项交叉试验将16例ARDS患者随机分配至接受IRV或不接受IRV。结果发现,IRV增加了平均气道压力,但PaO2的改善并未达到统计学意义(93mmHg vs 86mmHg)。IRV通常需进行深度镇静或神经肌肉麻痹,因为I:E反比是反常的且是不舒服的。在血流动力学方面,患者通常可良好耐受IRV。类型-IRV可在定压通气(PL-IRV)和定容通气(VL-IRV)过程中进行,两者并无明显的优劣之分。一项多中心随机试验在ARDS患者中比较PL-IRV和VL-IRV,发现IRV的类型并不影响死亡率。
定压通气-在PL-IRV中,IRV是通过增加I:E比直至吸气时间超过呼气时间来启动的。PC-IRV的主要优势是可保证不会超过最大气道平台压,这可能降低肺气压伤或呼吸机相关的肺损伤的风险。此外,许多临床医生认为,PC-IRV比VC-IRV更难产生有临床意义的自发性PEEP,但这尚未被证实。
定容通气-在定容通气中,可采用斜波(减速流)或方波(恒定流)的气流模式来启动IRV:当采用斜波时,初始设置的吸气峰流速至少是每分钟通气量的4倍,之后缓慢下降,直至吸气时间超过呼气时间时为止。当采用方波时,加入吸气末停顿(0.2秒可有较好的效果),之后慢慢延长,直至吸气时间超过呼气时间时为止。风险-在IRV时呼气时间较短,这可增加内源性PEEP和其不良后果(例如:肺气压伤和低血压)的风险(图 7)。IRV似乎也可增加与内源性PEEP无关的肺气压伤的风险。一项纳入14例采用PC-IRV进行机械性通气的患者的研究显示,虽然在这些患者中不存在可测量的内源性PEEP,但气胸的发生率仍为29%。
总结
机械通气模式是指吸气支持的方式。在定容通气时,当达到所设定的潮气量后停止送气。在定压通气时,当达到所设定的吸气压后停止送气。这两种模式均有各自独有的优缺点。压力支持通气(PSV)既不是定容通气,也不是定压通气。在这种模式下,一旦患者触发呼吸则会给予吸气压力,直至吸气流量降至预设的峰值百分比。持续气道正压通气(CPAP)是指给予持续的气道正压水平。双水平气道正压(BPAP)是一种在无创性正压通气(NPPV)期间使用的模式,其可给予预设的吸气相气道正压(IPAP)和呼气相气道正压(EPAP)。气道压力释放通气(APRV)模式是在持续高气道压(高P)和持续低气道压(低P)之间循环的模式。在APRV期间允许自主呼吸。这种模式的变型包括:间歇指令气道压力释放通气(IMPRV)和双水平间歇正压通气。反比通气(IRV)不是一种机械通气模式,而是一种在定容或定压机械性通气期间使用的策略。在IRV期间,吸气时间大于呼气时间(I:E比反向),这增加平均气道压力,并改善氧合。