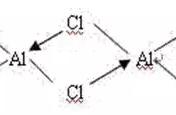
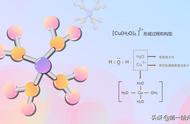
未来对DFT计算中计算二碳基结构的C-O伸缩振动的误差进行基准研究可能可以解决这个问题,从而解释了Ir(CO)2物种的对称伸缩频率在DFT计算中明显高于Ir一碳基物种,而在实验中却较低的差异。
然而,如下所述,由DFT计算得出的单碳基和二碳基Ir的氧化态与实验非常一致,进一步证实了在计算单碳基结构与二碳基结构的C-O伸缩振动时需要进行基准研究的必要性。总之,在反应机理的讨论中,单碳基/活性态将被表示为Ir(CO)(OL)(O)2。

为了更好地理解Ir1/TiO2上CO氧化的机理,进行了多种动力学测量,并结合原位光谱测量和DFT计算进行了补充。实验结果表明,在所有条件下,CO的级数是正的,而O2的级数在所有条件下接近于0。
CO的正级数表明在至少一个动力学相关步骤中涉及了气相CO或弱吸附CO,这被认为是一个Eley–Rideal型步骤(即一个真正的Eley–Rideal机理或类似的动力学机理,涉及第二个弱吸附CO分子)。

由于在CO氧化条件下鉴定出Ir(CO)(OL)(O)2作为最丰富的物种,Eley–Rideal型步骤可以是(a) Ir(CO)(OL)(O)2 CO ⇔ Ir(CO)2(OL)(O)2 → Ir(CO)(OL)(O) CO2或(b) Ir(OL)(O)2 CO ⇔ Ir(CO)(OL)(O)2 → Ir(OL)(O) CO2。
然而,Eley–Rideal型与原位DRIFTS结果不一致,原位DRIFTS结果显示在反应期间和反应后稳定存在Ir(CO)中间体,更重要的是,在无CO存在的情况下,在170 °C下反应20分钟。
在CO氧化反应中,Ir1/TiO2的CO氧化动力学和机理是复杂的。CO级数的变化和CO分压的影响提示CO在速率决定步骤中发挥了重要作用。

一个*CO似乎作为活性的Ir1复合物的一部分,只作为旁观配体参与反应。该工作在分子水平上对Ir1/TiO2上的反应循环进行了深入理解,旨在构建异相催化和均相催化之间的桥梁。