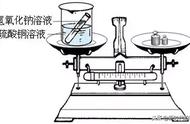
甲烷在空气中燃烧的化学方程式
通过甲烷燃烧的化学变化方程式,可以看出在化学变化前后,元素的种类没有发生改变,反应前的物质有甲烷和氧气,两种物质里共有碳、氢、氧三种元素,反应后生成的物质是二氧化碳和水,物质的种类发生了改变;然而两种生成物的组成元素种类没有发生改变,即也是碳、氢、氧三种元素;反应前后元素的种类没有发生变化。如何来理解“六不变”呢?可以从两个方面来加以理解,即宏观方面和微观方面。
首先宏观方面,是从物质和元素这两个方面来看。
①反应前后组成物质元素种类不会发生改变。
②反应前后每种元素的质量不会发生改变。
③反应前后物质的总质量不会发生改变
其次微观方面,主要是从原子方面来描述;因为原子是化学变化中的最小粒子。也就是说在化学变化中原子不会再发生改变,只是排列组合方式发生了变化,主要包括以下三个方面的意思。
①反应前后原子种类不会发生改变。
②反应前后每种原子的质量不会发生改变。
③反应前后每种原子的数目不会发生改变。

“六个不变”的详细图解
2、要牢记什么是“两个变”
在化学变化中到底哪些发生了改变呢?我们可以从化学变化的本质来分析,化学变化就是有新的物质生成(或是有新的分子生成)。“新的物质生成”,说明化学变化前后物质的种类发生了改变;新的分子生成”,说明化学变化前后分子的种类发生了改变。前面提到过,化学变化实际上就是构成物质的原子重新排列组合。

化学反应的本质
原子的排列方式发生了改变,也就是分子发生了改变,自然物质也就发生了改变。即质量守恒定律中的“两个变”
①化学变化前后物质的种类发生了改变。
②化学变化前后分子的种类发生了改变
3、要理解什么是“一个可能变”
对于化学变化前后,分子的数目是否发生改变?不好给出一个肯定的答案;有的化学变化,在变化前后分子的数目恰好不变;因为化学变化就是分子中的原子重新排列组合,这样就会存在组合前后分子数目恰好相等的情况,这一参数在研究化学变化过程意思不是很大,主要是偶然因素导致的结果。
三、如何避免用质量守恒定律解释化学变化的误区
中考化学中经常会出现这样的题目“蜡烛在空气中燃烧,质量在不停地减少,是不是这个化学变化不遵循质量守恒定律?如果遵循质量守恒定律,那么质量为什么还会减少呢?”。通过对历年的中考化学试卷分析,发现很多同学在这种题型上失分。考生如何做到在质量守恒定律的知识考题中不失分呢?不仅要求考生从宏观和微观方面理解质量守恒定律,也就是说“所有的化学变化都遵循质量守恒定律”;还要清楚物质反应前后的状态,具体来说就是以下三个方面。
1、如何用质量守恒定律来解释有气体参加或生成的反应
在化学反应中,有时候生成物中有气体物质出现;对于这种有气体生成的化学反应,如何来看待其质量守恒关系呢?这就跟这个反应的环境很有关系,如果是在敞开的环境进行的化学变化,随着反应的不断进行,生成的气体逸散到空气中,就会导致反应前后“物质的总质量不相等”。比如像刚才提到的蜡烛燃烧的反应,蜡烛的质量在减少,但是我们不能误认为这个反应不遵循质量守恒定律。如果用质量守恒定律来解释这个反应的话,应该是“参加反应的蜡烛的质量 参加反应的氧气的质量=生成的水和二氧化碳的质量”,而不能够单单从蜡烛的减少来否定质量守恒定律。

蜡烛在空气中燃烧的质量守恒定律的解释
对于有气体参加的化学反应,也会出现反应前后“物质的总质量不相等”。比如铜丝在空气中加热,反应前后“铜丝”的总质量会增加,为什么会出现这种情况呢?绝对不能轻易断言是“不遵循质量守恒定律”,反应后之所以会出现质量增加,是因为反应后生成的“铜丝”实际上是氧化铜,它的质量应该等于参加反应的铜丝的质量和参加反应的氧气的质量之和;所增加的“铜丝”的质量实际上就是参加反应的氧气中氧元素的质量。