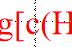拉乌尔定律(Raoult's law)是法国化学家弗朗索瓦·马利·拉乌尔(François-Marie Raoult)于1887年提出的一个定律,描述了在一个密闭系统中,理想溶液中组分气体分压与溶液中该组分摩尔分数之间的关系。

拉乌尔定律的数学表达式为:
πB = xB·P
其中,πB 是溶液中组分B的蒸气压,xB 是溶液中组分B的摩尔分数,P 是溶液上方的气相总压。
拉乌尔定律对于非理想溶液同样适用,但是需要引入一个校正因子α,以考虑非理想溶液中的相互作用。校正后的拉乌尔定律表达式为:
πB = α·xB·P
其中,α 是校正因子,其数值取决于溶液中各组分的性质和浓度。
拉乌尔定律在化学、化工、环境科学等领域具有广泛的应用,特别是在研究溶液性质、设计蒸馏分离过程等方面具有重要意义。
,