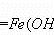胶体的性质
混凝去除的对象主要是胶体,胶体粒子的性质会影响混凝的效果。那么胶体有什么性质呢,下面主要通过结构,分类,稳定和凝聚四个部分进行讲解。
首先,胶体具有双电层结构。胶体微粒的中心叫做胶核,胶核的表面由于吸附、表面溶解等原因,会带有电荷,具有一定的电势。由于胶核带点,必然会存在静电引力,会吸引溶液中的异号离子向胶核表面趋近;由于异号离子本身还存在热运动和其它作用力,会远离胶核表面,向溶液中扩散。这两种力的综合作用下,使得靠近胶核表面处的异号离子浓度大,随着胶核表面距离的增加,异号离子的浓度逐渐减小至溶液中离子的平均浓度。电势形成的离子层和异号离子层就构成了胶体的双电层结构。

胶体双电层结构
由于胶核表面电势形成离子的静电引力很强,靠近胶核表面的部分反离子会紧附在胶核表面,跟随胶核一起移动,这一层反离子称为束缚反离子,与胶核形成了吸附层,吸附层本身只有几个离子的厚度;吸附层之外称为扩散层,由于静电离子引力减弱,在胶体微粒运动时,扩散层内的反离子会与胶体表面脱离,与液体一起运动,因此扩散层的反离子称为自由反离子。
通常,胶核与吸附层统称为胶粒,再加上扩散层则称为胶团。由于胶核表面的反离子总是比吸附层的多,所以胶粒是带电的,但是整个胶团是不带电的。其中胶核表面吸附的离子所形成的电势为总电势,称为φ电势;胶核在滑动时的电势,即滑动面上的电势为电动电势,称为ζ电势,一般将吸附层的边界视为滑动面。其中φ电势并没有实用意义,而ζ电势是表示胶体稳定性的一个重要指标,可以通过实验进行测定,ζ电势并不是一个定值,它会随着溶液温度、pH值及反离子浓度等外界因素的变化而变化。

胶体结构
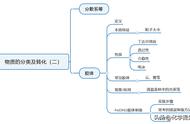
其次,根据胶核表面是否带有极性基团,胶体可分为不带极性基团的憎水胶体和带极性基团的亲水胶体。

胶体分类
憎水胶体的吸附层中,反离子直接与胶核接触;亲水胶体由于胶核表面极性基团的存在,对水分子具有良好的亲和性,会导致水分子优先吸附在胶核表面,形成一层水化膜。憎水胶体的双电层和亲水胶体的水化膜都有一定的厚度,这个厚度会影响到胶体的稳定性。
胶体最重要的一个性质,那就是胶体的稳定性(胶体粒子在水中保持分散悬浮状态的一种特性)。其实胶体溶液并不是真正的稳定体系,但是在水处理中,由于胶体在重力场的沉淀速度十分缓慢,那么有多缓慢呢,我们举一个例子:一个粒径1μm的粘土颗粒,在重力场中沉降10cm,大概就需要20个小时,而水处理的沉淀池一般只有几个小时的沉淀时间,胶体的沉降性基本可以忽略,因此胶体被近似的认为是稳定的。
胶体的稳定性主要与动力学稳定性和聚集性稳定性有关:

胶体的稳定性
如果胶体表面的电荷或水化膜消失,聚集稳定性也会随之消失,小颗粒胶体就有可能互相聚集成大的颗粒,从而导致动力学稳定性破坏,因此胶体稳定性的关键在于聚集稳定性。
胶体颗粒之间的相互作用能的关系,是由前苏联的德加根(Derjaguin)、兰道(Landon)和荷兰的伏维(Verwey)、奥贝克(Overbeek)四位科学家提出来的,因此我们把这个理论称为DLVO理论,由于DLVO理论是以憎水胶体为对象推导出来的,所以只适用于憎水胶体的情况。

胶体凝聚
上图即为胶体粒子之间距离与排斥势能和吸引势能的关系。
其中Emax为排斥能峰,当布朗运动的能量大于排斥能峰时,胶粒就有可能在布朗运动的推动下越过排斥能峰,进入吸引势能区域,从而发生碰撞和凝聚,当然了,布朗运动的能量通常要比排斥能峰小很多,所以一般情况下,胶粒并不能自发地发生碰撞和凝聚。
由于排除能峰的存在,只有当胶粒间的距离<OA时,胶粒才会发生碰撞和凝聚,由此也可以推断出,造成胶体稳定性的主要原因是胶粒之间存在排斥能峰,如果降低这个排斥能峰,就可以引起胶体颗粒间发生碰撞、脱稳,最后形成絮凝体。而降低排斥能峰的关键就是降低胶体的ζ电势,即降低胶粒间的静电斥力,向胶体溶液中投加电解质就是一个降低静电斥力的好方法。