=0.3 mol·L-1·s-1;
同理可知:v(B)=0.15 mol·L-1·s-1;
2 s时A的转化率=

2 s时B的浓度为0.7 mol·L-1;即B项错误。
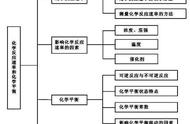
【板书】6.反应速率的测定方法
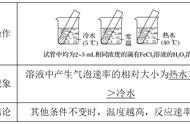
【讲述】测定化学反应速率的关键是测定某一时间间隔内反应体系中某物质浓度的变化。物质的某些物理性质(如压强、体积、吸光度、电导率等)与其物质的量或浓度存在函数关系,因此人们常用物理方法,通过准确而快速地测定反应物或生成物浓度的变化来确定化学反应速率。常用的物理方法有量气法、比色法、电导法。
【课堂小结】


本节内容实在必修第二册的基础上的进一步加深,多数知识和内容是对必修内容的复习和回顾,因此在教学中侧重对化学反应速率计算练习。