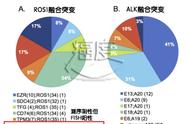
ROS1融合
ROS1基因的突变形式是与其他的基因发生融合,这种融合造成了一个新的基因,从而使细胞癌变。
出现ROS1突变的患者,更多的是年轻的、非吸烟的肺癌患者,其中肺腺癌居多。突变者约占 NSCLC 总数的 3%。常见的融合伴侣为G2032R。
由于ROS1融合基因的结构和功能与ALK融合基因存在众多相似性,因此运用于ALK融合基因突变的靶向药克唑替尼对ROS1融合阳性的非小细胞肺癌患者也有效。在ROS1基因重排的非小细胞肺癌患者中使用克唑替尼,表现出理想的抗肿瘤活性,客观缓解率(ORR)能够达69.8%。2019 V2版肺癌NCCN指南更新,将ROS1的检测地位提高,作为晚期肺腺癌和部分鳞癌初治检测中必须检测的基因。FDA批准治疗ROS1阳性的药物有克唑替尼、Entrectinib,此外治疗ROS1融合的药物还有色瑞替尼,卡博替尼,劳拉替尼,TPX005,以及DS-6051b。

▲表5 肺癌ROS1突变可用靶向药物

KRAS突变
KRAS是RAS家族的一员。KRAS的突变会持续刺激细胞生长,并阻止细胞死亡,从而导致肿瘤的发生。肺腺癌里的KRAS突变频率约为25%,鳞癌里KRAS基因突变频率为5%。
腺癌、吸烟史及白色人种是KRAS突变的危险因素。
虽然KRAS突变有很大的发生率,但长期以来的研究证实它是一种“不可摧毁的”蛋白质。这是因为这种蛋白质缺乏明显的靶点可以让小分子药物可以结合并损害其功能。针对KRAS突变的患者,研究重点都集中在阻断KRAS的下游通路上,如MEK,CDK4/6以及免疫治疗,主要有以下三种治疗方式:
①MEK抑制剂联合化疗:曲美替尼/司美替尼(单用疗效有限)联合化疗
②CDK4/6抑制剂:Abemaciclib
③免疫治疗(KRAS突变肿瘤TMB较大,PD-L1表达较高)
直到2019年ASCO上,一款新药AMG510攻破了KRAS这个坚硬的堡垒,疾病控制率达到了100%,震撼了整个肿瘤界。
①经过三十年的RAS研究,AMG 510是第一个达到临床阶段的KRASG12C抑制剂!
②首次人体结果显示KRAS突变实体瘤的初步安全性,耐受性数据和抗肿瘤活性!
FDA批准AMG 510孤儿药物指定用于KRASG12C阳性非小细胞肺癌和结肠直肠癌,在肺癌中20%的KRAS存在G12C突变,AMG510打开了历史性的缺口。

MET异常
MET也是非小细胞肺癌比较常见的突变,外显子14跳跃突变检出率达3-4%。
目前针对MET基因异常的药物较多,克唑替尼及卡博替尼在临床中应用比较普遍,除此两种高选择性MET抑制剂tepotinib和capmatinib(INC280)在MET外显子14(MET ex14)突变的晚期非小细胞肺癌患者的一线和二线治疗中显示出良好的临床活性。