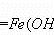又到了大家最爱的实战环节了,刚学到这么多新姿势马上就能用上,想想还有些小激动呢。这道题挺简单的,我们就一起来看吧,选择叙述正确的。
A选项,溶液是电中性的,胶体是带电的。刚才我们已经讲过了,带电的是胶体中的分散质微粒也就是胶体粒子,而胶体本身是不带电的,另外我们刚才还讲了豆浆、牛奶、粥等都属于胶体,要是胶体带电的话,内咋滴喝碗汤还能整出触电的赶脚啊?
B选项,通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质只向某一极移动。这个选项有比较有迷惑性了,因为对于可以解离出离子的溶质,确实是溶质粒子分别向两极移动,胶体也正如题中所讲的只会向一极移动,那么这个选项的问题出在哪了呢?出在了前半句上,溶液中不仅有溶质为离子的溶液,还有溶质为分子的溶液,例如蔗糖溶液,而对于蔗糖溶液来说,通电后蔗糖分子是不会移动的。所以B选项也是错误的。
C选项,溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动。这个选项就纯属瞎扯了,还好布朗已经死了,要不他肯定会被气死。不论是胶体还是溶液,分散剂分子都在不停的做无规则运动。布朗运动是因为分散剂分子对分散质粒子不停的无规则撞击所引起的,而并非粒子本身的运动,是分散剂分子的无规则运动。
D选项是正确的,只有胶体才有丁达尔效应,可以用来鉴别胶体。
所以这道题,选D。

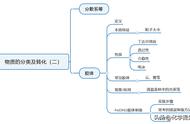
来看本节的最后一个部分,胶体的聚沉。

在前面第一部分我们就讲了胶体的介稳定性,这是指胶体的稳定性介于溶液和浊液之间,在一定条件下能够稳定存在,属于介稳体系。胶体能够保持介稳态的原因有两个,分别是胶体粒子带电和布朗运动。由于同种胶体离子的电性相同,在通常情况下,它们之间的相互排斥阻碍了胶体粒子变大,使其不易聚集。同时胶体粒子所做的布朗运动也使得它们不容易聚集。

胶体粒子的带电规律,不同的胶体粒子所带的电性也不同,这就像不同的同学有不同的兴趣爱好一样,有的同学喜欢运动,有的同学喜欢音乐,还有的同学就喜欢自己同桌。
一般来说金属氢氧化物、金属氧化物胶粒带正电。这是因为这类胶粒常吸附它的组成离子中的阳离子。如Fe(OH)3胶粒吸附的是Fe3 。
非金属氧化物胶体通常带负电,这是因为非金属胶粒常吸附它的组成离子中的阴离子。如硅酸胶体的胶体粒子吸附的是硅酸根离子(SiO32-)。
AgI胶体就像一位可盐可甜的同学,时而温柔、时而霸道。在AgI胶体中,若I-过量,胶粒吸附I-而带负电;若Ag 过量,胶粒则吸附Ag 而带正电。