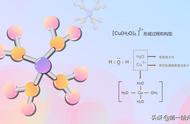
NaCl晶体中,每个离子被处在正八面体6个顶点带相反电荷的离子包围,Cl-离子和Na 离子的配位数都为6。
注意:每个Cl-(Na )离子周围等距且紧邻的Cl-(Na )在上、中、下层4个,共12个,这不是真正的配位数。因为是同电性离子。
又如金属晶体中的简单立方堆积(如图所示),

Po晶体中,立方体位于1个顶点原子的上下、前后、左右各有2个原子与其形成金属键,配位数为6。
4.配位数为4的几种晶体。
如ZnS型离子晶体(如下图所示),

ZnS晶体中的S2-离子和Zn2 离子排列类似NaCl型,但相互穿插的位置不同,使S2-、Zn2 离子的配位数不是6,而是4。具体可将图示中分为8个小立方体,其中体心有4个S2-离子,每个S2-离子处于Zn2 离子围成的正四面体中心,故S2-离子的配位数是4。以大立方体的面心Zn2 离子分析,上、下层各有2个S2-离子,故Zn2 离子的配位数为4。Zn2 离子的配位数不易观察,亦可利用ZnS的化学式中的离子比为1∶1,推知Zn2 离子的配位数为4。
又如金刚石、碳化硅等原子晶体(如图所示),

与ZnS型离子晶体类似情况,配位数均为4。二氧化硅原子晶体中,Si与O原子形成的是硅氧四面体(图示略),Si的配位数为4,而SiO2的原子比为1∶2,故O的配位数是2。
再如CaF2型离子晶体(如下图所示),