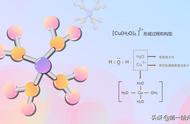
F-和Ca2 离子的配位数分别4和8。具体分析:每个F-离子处于Ca2 离子围成的正四面体中心,故F-离子的配位数是4。以大立方体的面心Ca2 离子分析,上、下层各有4个F-离子,故Ca2 离子的配位数为8。亦可利用CaF2的化学式中的离子比为1∶2,推知Ca2 离子的配位数是8。
还如在砷化镓晶胞结构(如图所示),

小黑点为镓原子,其配位数为4,砷化镓原子比为1∶1,故As原子的配位数也是4。
5.配位数为3的层状晶体。
如石墨或六方氮化硼等(图示略)。
6.链状结构的配位数为2。
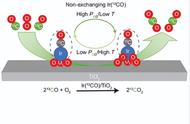
如硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示。Ti、O原子的配位数均为2。

注意:由于晶体结构对称性关系,晶体中不可能有11、10、9、7、5的配位数。晶体中最高配位数为12。