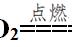例题,含0.2 mol NaOH的烧碱溶液,在标况下吸收CO2气体3.36L,所得溶液中含有什么物质(不考虑水),其物质的量各为多少?
老规矩,暂停视频,假装思考三分钟。
假装完了,我们一起来看。如果没有前面的视频给大家酝酿一下便便,哦不,酝酿一下这道题,而是直接给出这道伤害不大,但侮辱性极强例题,一定会有不少同学自信满满的答道,so easy! 体系里还剩过量的二氧化碳和生成的碳酸钠。但是过量的二氧化碳还能继续和碳酸钠生成碳酸氢钠呢,没想到吧,小丑竟然是你自己,后浪,耗子尾汁呀。
来看无聊的解题过程吧,友情提示一下,如果你还在厕所里蹲着,差不多可以出来了。再蹲一会腿麻了可能就出不来了呢,亲~。
第一步,求二氧化碳物质的量,题目中给出了标况下二氧化碳的体积,计算得到二氧化碳物质的量。
接下来我们就要判断是否能够恰好反应完全,以及谁过量的问题。我们可以假设其中的任意一种物质完全反应,计算另一种物质所需的量,即可判断哪种物质过量。演示中,我们假设NaOH完全反应,求所需的CO2的量,刚刚讲过的一般解题步骤应该也忘得差不多了吧,正好一起来复习一遍,首先写出反应方程式,标出相关量,
接下来,设未知数,现在我们要求CO2的物质的量,所以可以设CO2物质的量为n(CO2),当然,假设的这一步很多时候可以省略。
之后列出比例式,并解得未知数n(CO2),这里我们直接给出了结果,大家自己解题的时候建议写全。
计算得到,若氢氧化钠完全反应,需消耗二氧化碳0.1 mol,
0.1<0.15,因此二氧化碳过量。假如这里计算得到的数大于0.15的话,那说明是(语气放慢)对,氢氧化钠过量。
所以,题目中二氧化碳过量,氢氧化钠完全反应后还剩过量的CO2 0.05 mol未反应。
并且,我们还需要根据完全反应的NaOH求出生成的碳酸钠的量为0.1 mol。
到这一步可以先做一个小节,氢氧化钠完全反应,二氧化碳过量,并且有碳酸钠生成,因此此时体系中还剩过量的二氧化碳和生成的碳酸钠。到这里还不能掉以轻心,因为二氧化碳能够和碳酸钠继续反应生成碳酸氢钠。

同样,首先,写出第二步的反应方程式,并标出相关量。
根据刚才的计算我们很容易可以看出,此时体系中碳酸钠过量。因此这一步计算应该按照二氧化碳的量来算。
分别假设反应消耗的碳酸钠和生成的碳酸氢钠为n(Na2CO3)’和n(NaHCO3),计算得到两者物质的量分别为0.05 mol和0.1 mol。
此时,体系中的二氧化碳消耗完全,体系中只剩过量的碳酸钠和生成的碳酸氢钠。

最后,把两步反应放在一起可以得出结论。
最终体系中只含有两种物质,即Na2CO3和NaHCO3 ;
其中Na2CO3的量为第一步生成的量减去第二步反应的量,即为0.1 – 0.05 = 0.05 mol; NaHCO3 为0.1 mol。

讲完了既难讲又难听懂的例题,我们来看点令人心情愉悦的理论知识吧,大家不必担心,后面还有好几道例题,保证能把大家恶心的透透的。
4、化学计算的特殊方法。(1)差量法。根据反应前后物质相关量发生的变化,找到“理论差量”,可以是反应前后的质量差、物质的量差、气体体积差等,该差量的大小与反应物的有关量成正比。
相信如果没学过这一方法会看的一头雾水,不如直接看索然无味的例题吧。
例题,铁粉与高温水蒸气完全反应后得到的干燥固体的质量比反应前铁粉的质量增加32 g,问参加反应的铁粉物质的量?
这道题看起来还真是有点棘手呢,不管题目好做与否,第一步写出反应方程式肯定不会错。